HIV: cientistas descobrem nova variante do vírus em circulação no Brasil
A linhagem circula em pelo menos três das cinco regiões brasileiras: Sul, Sudeste e Nordeste
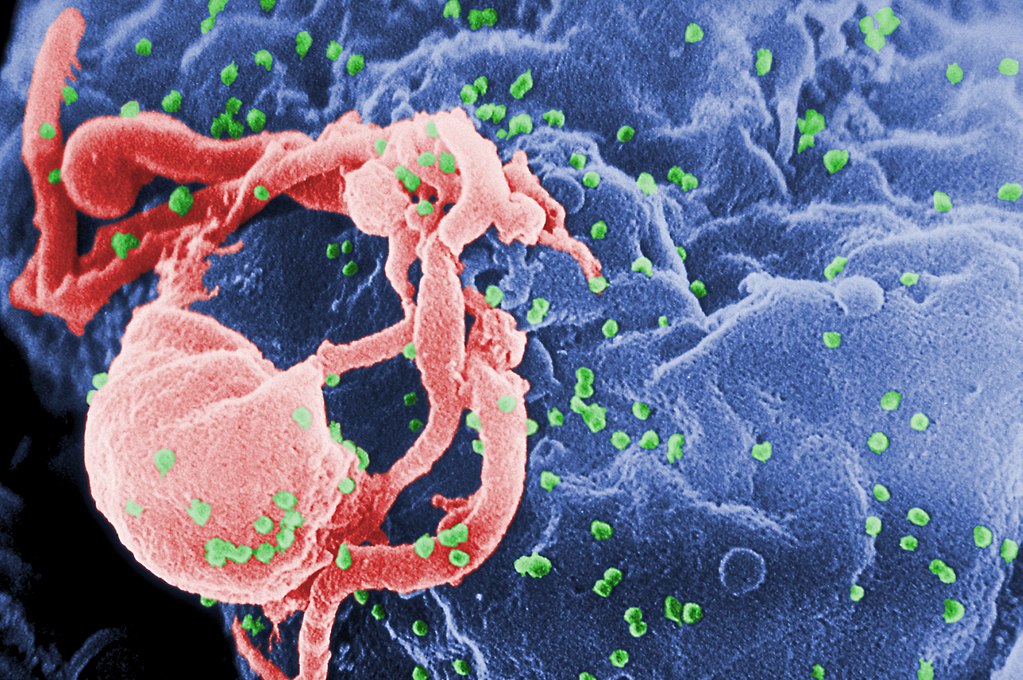
Cientistas brasileiros identificaram uma nova variante do HIV, vírus que sem o tratamento adequado pode, em último estágio, levar ao desenvolvimento da aids.
O recombinante é fruto de uma mistura genética de dois tipos de HIV-1, chamados B e C. A linhagem circula em pelo menos três das cinco regiões brasileiras: Sul, Sudeste e Nordeste.
Vale reforçar que não se trata de um novo subtipo viral, mas uma nova Forma Recombinante Circulante (CRF, em inglês), que são derivadas de episódios de dupla infecção ou de reinfecção.
Os achados são de um estudo conduzido por pesquisadores da Universidade Federal da Bahia (UFBA) e da Fundação Oswaldo Cruz (Fiocruz) publicado na revista científica Memórias do Instituto Oswaldo Cruz. As informações foram adiantadas pela Agência Bori.
O vírus foi detectado em uma avaliação mais ampla, sobre subtipos de HIV-1 circulantes na Bahia. De acordo com a doutora em biotecnologia Joana Paixão Monteiro-Cunha, professora da UFBA e uma das coordenadoras do estudo, a descoberta motivou uma análise mais aprofundada, comparando-o com sequências de linhagens recombinantes derivadas dos tipos B e C previamente descritas no mundo.
+ Leia também: Virada de jogo: evolução da medicina revoluciona o tratamento do HIV
“Assim, encontramos outros três vírus que apresentavam a mesma estrutura genética daquele encontrado na Bahia. Estes haviam sido isolados nos estados do Rio Grande do Sul e Rio de Janeiro. Também foi constatado que esses quatro vírus possuíam origem comum, ou seja, eram descendentes de um mesmo ancestral“, detalha Joana.
O estudo avaliou amostras de quatro pacientes, coletadas entre 2007 e 2019. Nesse contexto, os pesquisadores concluem que a variante surgiu, foi transmitida e se disseminou por diferentes regiões geográficas do país desde então. Contudo, mais pesquisas são necessárias para determinar outros pontos, como o local exato de origem.
Para Joana, esse resultado aponta que casos de reinfecção devem estar ocorrendo com certa frequência pois o “encontro” dos tipos B e C (ou outros) no organismo pode dar origem a uma linhagem recombinante. “A nova infecção para um indivíduo vivendo com o HIV-1 pode trazer impactos para o tratamento, uma vez que o vírus pode apresentar mutações associadas com resistência aos medicamentos antirretrovirais”, frisa Joana.
A doutora em biologia celular e molecular Monick Lindenmeyer Guimarães, pesquisadora do Instituto Oswaldo Cruz (IOC/Fiocruz) e também coordenadora da investigação, afirma que os achados são relevantes para o monitoramento do cenário epidemiológico do HIV no país.
“Novas variantes podem acumular características genéticas que favoreçam a transmissibilidade, o impacto na carga viral, na progressão para aids, e na aquisição mais rápida de mutações de resistência. No entanto, estudos ainda são necessários para confirmar esses possíveis efeitos”, destaca Monick.
+ Leia também: HIV: a importância do conceito “indetectável = intransmissível”
Como surgem as variantes do HIV?
“Os recombinantes surgem quando um indivíduo contrai mais de uma variante viral. Por exemplo, um vírus do subtipo B e um vírus do subtipo C. Quando eles infectam a mesma célula, ela pode gerar vírus híbridos e, a partir destes, os recombinantes”, afirma.
Variantes dessa natureza são comuns. Estima-se que cerca de 20% dos casos de HIV-1 no mundo sejam causados por vírus recombinantes. Desde o início da epidemia na década de 1980, mais 150 CRFs foram identificadas no mundo. O alvo do estudo brasileiro, por exemplo, recebeu a designação oficial de CRF146_BC.
Até o momento, o HIV-1 é classificado em quatro grupos M, N, O e P – sendo o M mais disseminado e principal responsável pela pandemia. Dentro deste grupo, são descritos dez subtipos (A, B, C, D, F, G, H, J, K e L), estes ainda podem sofrer eventos de recombinação como o documentado no novo artigo.
Os subtipos mais prevalentes no Brasil são o B, o F e o C e diversas formas recombinantes BF e BC, com variações de frequência em cada região geográfica. Estas combinações são classificadas em formas recombinantes únicas ou circulantes (CRFs).
“As CRFs são classificadas quando encontradas em pelo menos três indivíduos infectados e sem relações epidemiológicas entre eles”, pontua Joana.

Os resultados da análise devem ser interpretados com cautela uma vez que as informações disponíveis sobre os efeitos das alterações genéticas são escassas. Não se sabe, por exemplo, se a variante pode apresentar vantagens adaptativas ou replicativas.
“Mais estudos para analisar o comportamento desses vírus seriam necessários. Nesse caso, ensaios celulares poderiam contribuir”, diz Joana.
Da mesma forma, não existem evidências sobre o impacto do recombinante para o tratamento realizado no Brasil. “Parece que os subtipos de HIV-1 não apresentam grandes diferenças na resposta à terapia antirretroviral”, diz Joana.
“Mas é necessário o monitoramento contínuo, pois pode ser que algumas formas tenham mais probabilidade de sofrerem mutações que levam à resistência aos fármacos”, acrescenta Monick.
As pesquisadoras ressaltam que o surgimento de variantes genéticas distintas do HIV deve servir de alerta para a vigilância do vírus. Além disso, deve motivar avaliações da necessidade de atualização dos testes de triagem para detecção do vírus e do monitoramento de eficácia do tratamento.
+ Leia também: A lista de vacinas recomendadas para pessoas que vivem com HIV
Importância da genômica
Conhecer os meandros genéticos do HIV é uma estratégia importante em saúde pública.
Nesse contexto, o exame de genotipagem é imprescindível em casos de falha da terapia antirretroviral, além de ser utilizado em contextos específicos para o início do tratamento de gestantes, crianças e pacientes que apresentam coinfecção com tuberculose.
Em âmbito coletivo, a pesquisadora da Fiocruz afirma que o monitoramento de mutações que podem levar à resistência às drogas é de suma importância e deve ocorrer de forma geral, independentemente da variante viral.
“Este monitoramento deve ser realizado permanentemente em pessoas vivendo com HIV recém-infectadas, a fim de se verificar o percentual de mutações que têm sido transmitidas, pois se alcançarmos um patamar de 15% , de acordo com a OMS, teremos que incorporar o rastreio destas mutações pela genotipagem prévia ao tratamento”, pontua.
+ Leia também: Sorofobia: entenda como a discriminação impacta pessoas que vivem com HIV
Acesse as notícias através de nosso app
Com o aplicativo de VEJA SAÚDE, disponível para iOS e Android, você confere as edições impressas na íntegra, e ainda ganha acesso ao conteúdo dos apps de todos os títulos Abril, como Veja, Claudia e Superinteressante.




 Botox sem agulha: sérum promete mimetizar efeitos da toxina
Botox sem agulha: sérum promete mimetizar efeitos da toxina Gatos ficam de luto por outros animais da casa
Gatos ficam de luto por outros animais da casa Quer perder barriga? Esses 7 exercícios podem ajudar
Quer perder barriga? Esses 7 exercícios podem ajudar Tucumã: fruta da Amazônia é recordista em vitamina A
Tucumã: fruta da Amazônia é recordista em vitamina A Nimesulida: o que é, para que serve, como tomar e cuidados
Nimesulida: o que é, para que serve, como tomar e cuidados





![[BF2024-PRORROGAMOS] - Paywall - DESKTOP - 728x90](https://saude.abril.com.br/wp-content/uploads/2024/12/BF2024-PRORROGAMOS-Paywall-DESKTOP-728x90-2.gif)
![[BF2024-PRORROGAMOS] - Paywall - MOBILE - 328x79](https://saude.abril.com.br/wp-content/uploads/2024/12/BF2024-PRORROGAMOS-Paywall-MOBILE-328x79-1.gif)