1. O que são os biossimilares
Até o início dos anos 1980, não tinha jeito: se você precisasse de um medicamento de origem biológica, que não podia ser sintetizado em laboratório, precisava encontrá-lo de alguma forma na natureza. Um exemplo é a insulina. Fundamental para os tratamentos do diabetes, era extraída de porcos ou bovinos. Depois, era purificada, processada e, então, utilizada por quem precisava dela. Tudo começou a mudar em 1982, quando a insulina humana de produção industrial foi aprovada para uso pela primeira vez, dando início a uma revolução que, agora, começa a ganhar cada vez mais destaque.[1]
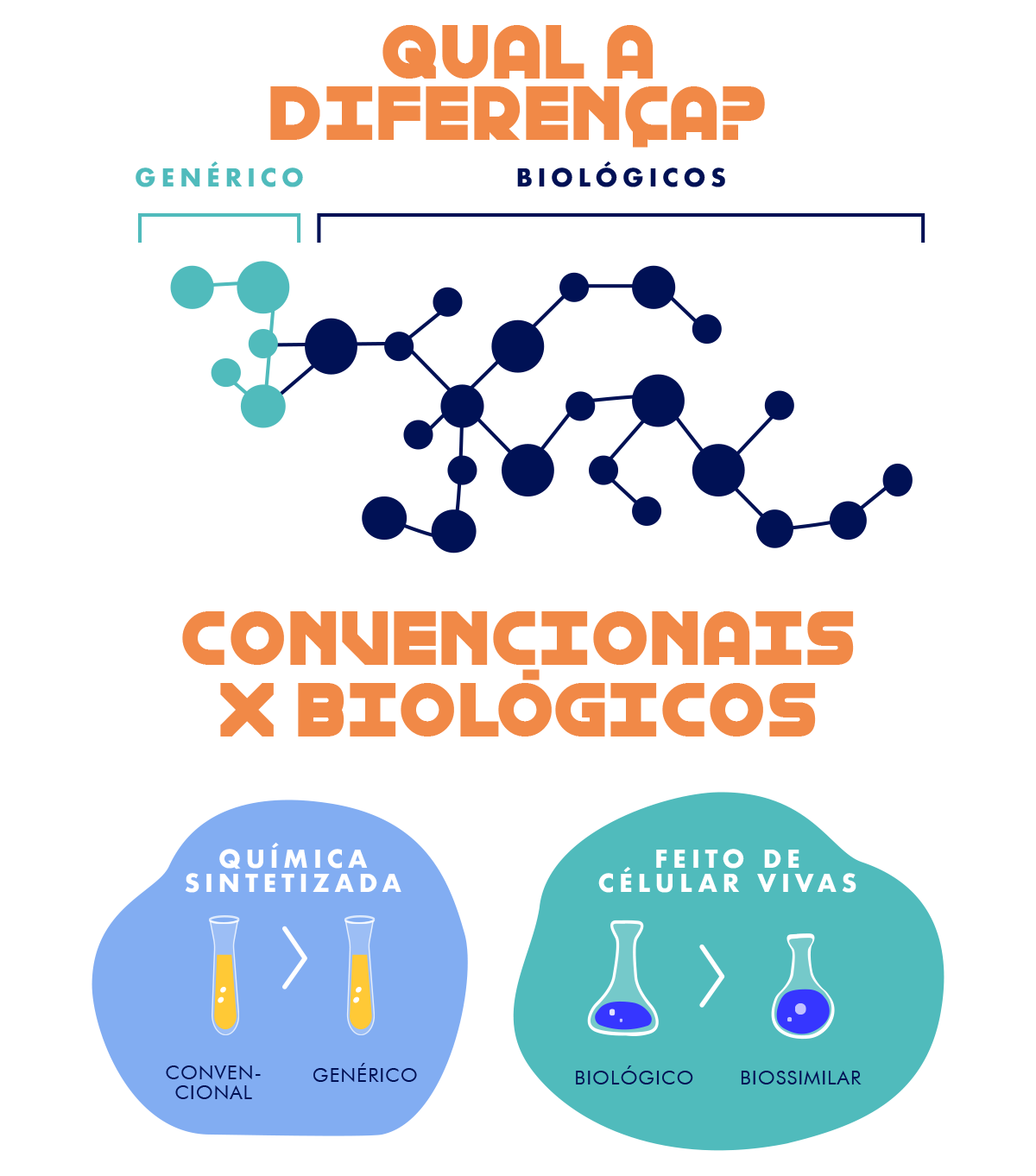
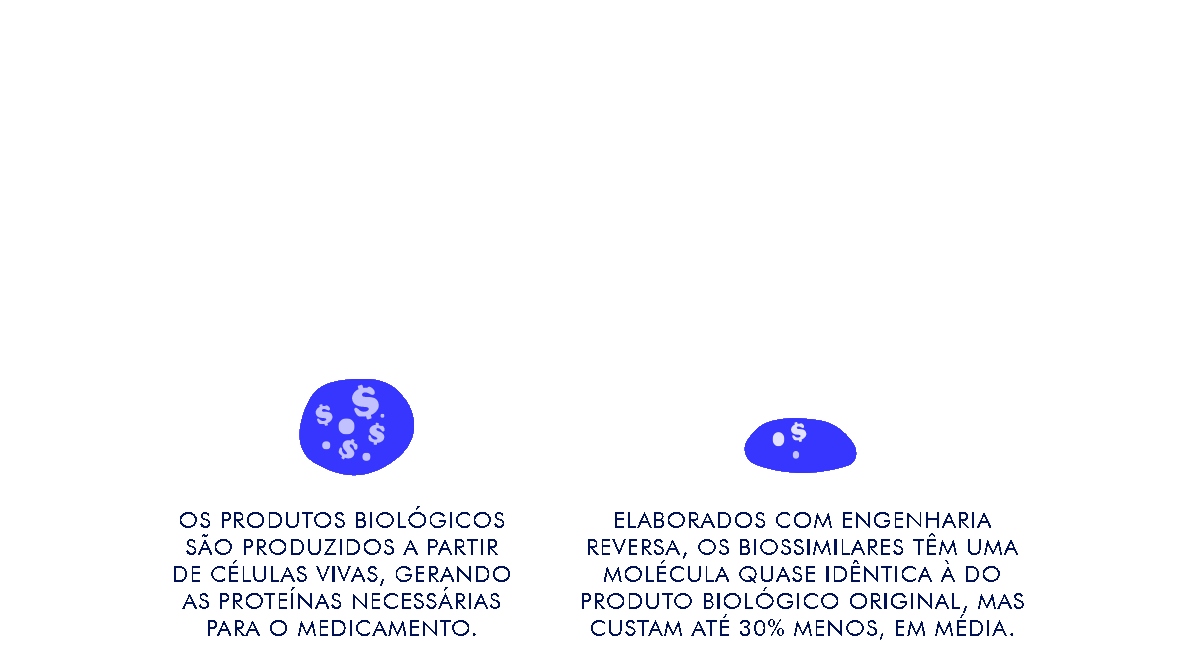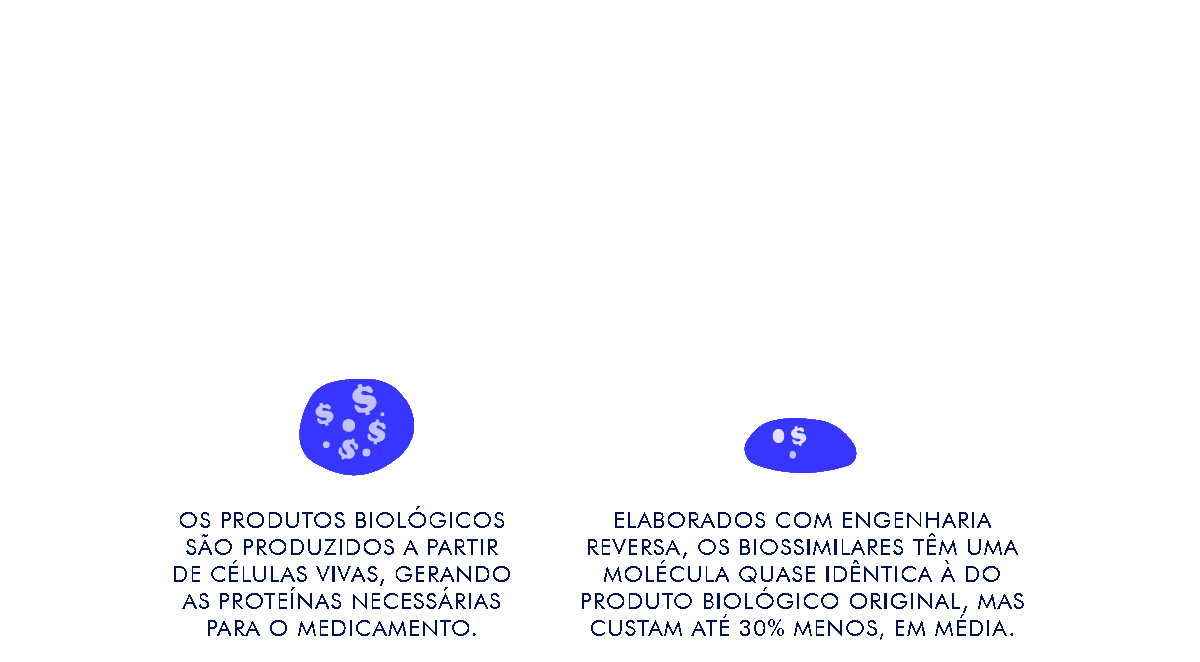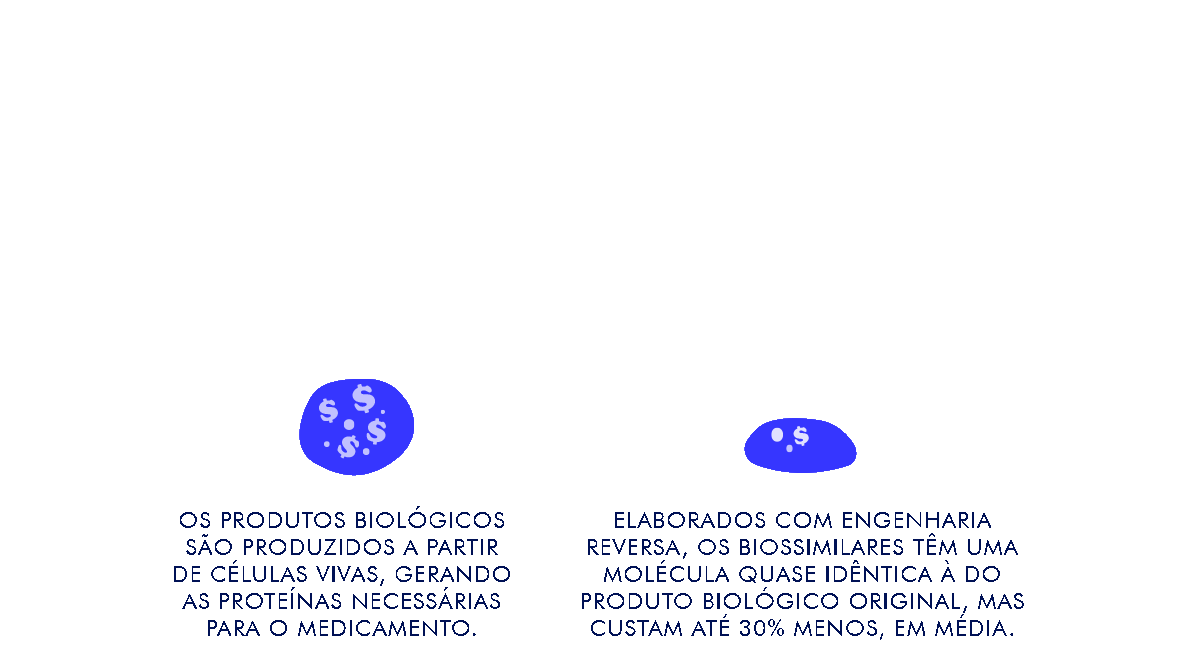
O nome já dá uma pista: os biossimilares têm esse nome por serem altamente similares aos produtos biológicos que os inspiraram. Você está começando a ouvir falar cada vez mais deles porque, nos últimos anos, novas possibilidades se abriram. Quando uma patente expira e com ela a exclusividade sobre o produto, diversos laboratórios podem produzir suas próprias versões, a um custo menor. Para isso, utilizam-se de um processo conhecido como engenharia reversa: os pesquisadores sabem onde querem chegar e, a partir do produto final, buscam compreender as maneiras de construí-lo.[2]
O produto, no caso, deriva de moléculas complexas de proteína, que podem ser usadas para tratar diferentes doenças – como o próprio diabetes ou a doença de Crohn, por exemplo. O resultado pode não ser totalmente idêntico (daí o “similar”), exatamente por se tratar de uma molécula biológica, mas isso não afeta sua capacidade terapêutica. “São feitos muitos testes para provar que a similaridade não é apenas pelo fato de a molécula ser muito parecida com a original, mas também em termos de eficácia e segurança”, explica o reumatologista Valderílio Feijó Azevedo (CRM-PR 12.199), professor da Universidade Federal do Paraná (UFPR) e um dos maiores experts em biossimilares no Brasil.
(Abril Branded Content/Abril Branded Content)
Em linhas gerais, os biossimilares são “cópias muito semelhantes” regulamentadas de produtos biológicos cuja patente já expirou, seguros e muito mais baratos que os originais.[3] “A principal razão para se investir neles é custo menor”, explica Azevedo. O processo de engenharia reversa exige menos gastos em pesquisa e desenvolvimento e, com isso, o usuário final não precisa pagar tão caro. Em média, os custos diminuem entre 20% e 30%, mas em alguns casos a economia pode ser ainda maior. “Entre 1% e 2% dos produtos utilizados no Brasil são biológicos, mas eles correspondem a quase metade do orçamento de medicamentos do país. Eles são muito caros”, diz o médico da UFPR.
Com os biossimilares, regulamentados pela Anvisa no Brasil desde 2010, mais pacientes podem ser tratados sem que o gasto aumente. Para cada vez mais doenças.
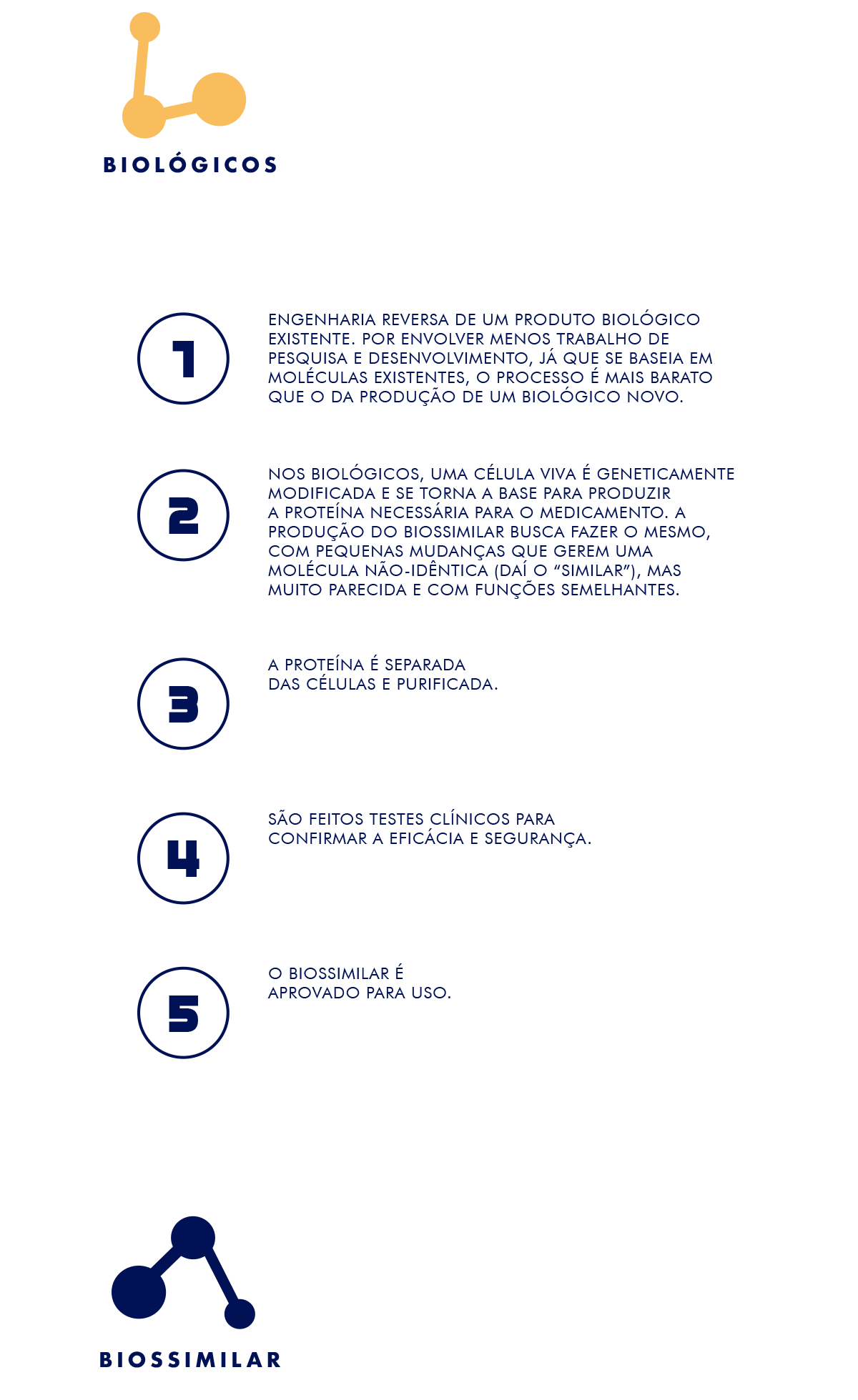
(Abril Branded Content/Abril Branded Content)